


Číslo 6 / 2012
Scintigrafie ledvinového graftu
Souhrn: Scintigrafie graftu je modifikací klasické dynamické scintigrafie ledvin a spočívá v bolusové aplikaci radiofarmaka (MAG-3 značený 99mTC), které se dobře vylučuje tubulárním systémem. Vyšetření umožňuje sledování perfúze štěpu (graftu), sekrece a exkrece do dutého systému, případně reziduální funkci autologních (vlastních) ledvin. Vedle ostatních zobrazovacích metod napomáhá v diagnostice možných pooperačních komplikací a kontrole efektu léčby pooperačních komplikací. Připojená kazuistika popisuje případ 75leté pacientky, která byla od roku 2004 sledována pro glomerulonefritidu, cysty ledvin a oboustrannou nefrolitiázu. Z důvodů diabetické nefropatie s renální insuficiencí bylo přistoupeno k transplantaci ledviny.
Klíčová slova: scintigrafie graftu – scintigrafie transplantované ledviny – rejekce ledvinového graftu.
Renal graft scintigraphy
Summary: Renal graft scintigraphy is a modification of classical dynamic renal scintigraphy. It is based on bolus application of radiopharmaceuticals (MAG-3 labeled with 99mTC), which is well excreted by tubular system. This examination can evaluate graft perfusion, secretion and excretion to the tubular system, eventually residual function of autologous kidneys. In addition to other imaging methods it helps in the diagnostics of possible postoperative complications and efficiency of their treatment. There is added case report of 75 years old woman, who was observed for the glomerulonephritis, renal cysts and bilateral nephrolithiasis. From the reason of diabetic nephropathy with renal insufficiency there were proceeded to the renal trasplantation.
Key words: renal graft scintigraphy – renal transplant scintigraphy – renal graft rejection
Úvod
Historie české transplantační medicíny začíná na počátku 60. let. První transplantace ledviny v tehdejším Československu byla provedena v Hradci Králové v roce 1961. V roce 1966 byl zahájen úspěšný transplantační program v Praze (Institut klinické a experimentální medicíny – IKEM). Transplantace ledvin byly prováděny téměř výhradně od žijících dárců. Až koncem 70. let došlo k vývoji nových imunosupresiv a k rozvoji transplantací ledvin i od zemřelých (kadaverózních) dárců. V současné době existuje v České republice sedm transplantačních center: IKEM, Praha, Fakultní nemocnice Motol, Praha, Centrum kardiovaskulární a transplantační chirurgie Brno, Fakultní nemocnice Plzeň, Fakultní nemocnice Hradec Králové, Fakultní nemocnice Olomouc a Fakultní nemocnice Ostrava.
Dynamická scintigrafie transplantované ledviny
Tato zobrazovací metoda je modifikací klasické dynamické scintigrafie ledvin. Spočívá v intravenózní bolusové aplikaci radiofarmaka (99mTC MAG-3). Vyšetření umožňuje rychlou informaci o perfúzi, separaci funkce štěpu (graftu) a reziduální funkci autologních (vlastních) ledvin. Nebyl-li důvod k nefrektomii, vlastní ledviny pacientům zůstávají v původní lokalizaci. Taktéž při možné další transplantaci, nedošlo-li k rejekci a následné nekróze, původní transplantovaná ledvina se nevyjímá. Jsou-li k transplantaci použity dětské ledviny, jsou dospělé osobě transplantovány většinou obě ledviny. Vedle ostatních zobrazovacích metod, jako jsou např. ultrasonografie (USG), počítačová tomografie (CT), nukleární magnetická rezonance (NMR), angiografie, intravenózní vylučovací urografie (IVU), napomáhá scintigrafie graftu v diagnostice pooperačních komplikací.
Scintigrafické vyšetření graftu provádíme na naší klinice nukleární medicíny převážně na detašovaném pracovišti ve vyšetřovacím monobloku interní kliniky. Zánik či zhoršení funkce štěpu nastává i z neimunitních příčin, jako jsou infekce, onemocnění transplantované ledviny jiným nefrologickým onemocněním, uzávěrem cév atd. Banální zdravotní problémy mohou signalizovat významnější zdravotní problém, a proto vybudování detašovaného pracoviště je pro samotného pacienta velkým přínosem. Především se na minimum zkrátila doba převozu pacienta na vyšetření a zpět na jednotku intenzivní péče (JIP). Pacient není delší dobu vystaven vnějším vlivům, jako jsou chlad, průvan či možnost vzniku nozokomiální nákazy od ambulantních pacientů, které by mohly ohrozit jeho už tak oslabený imunitní systém.
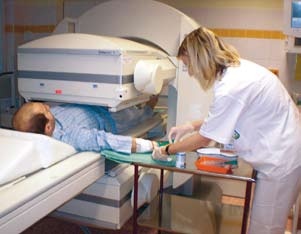
Vyšetření provádíme pomocí dvouhlavé gamma kamery E-CAM. Poloha pacienta je vleže na zádech. Transplantovaná ledvina je voperována pacientovi do pravé nebo levé jámy kyčelní, a proto detektor scintigrafické kamery nastavujeme nad oblast břicha pacienta tak, aby byla zachycena oblast transplantované ledviny, ilických arterií a močového měchýře. Lékař pacientovi aplikuje intravenózně ve formě bolusu 300 MBq MAG-3 (merkaptoacetyltriglycin) značený 99mTC (technecium). Toto radiofarmakum je dobře vylučováno tubulární sekrecí. Čerstvě transplantovaní pacienti mívají zajištěnou centrální žílu (vena subclavia nebo vena jugularis interna), do které může lékař radiofarmakum aplikovat. Většina pacientů je v chronickém dialyzačním programu a mívají našitu jednu a více arterio-venózních spojek (A-V shuntů). Zde je možná stagnace radiofarmaka, a proto do nich radiofarmakum nikdy neaplikujeme. Pokud nemá pacient zajištěn žilní vstup, zavádíme flexibilní kanylu napojenou na prodlužovací hadičku do antekubitální žíly. Pacienti těsně po transplantaci mívají většinou ještě zaveden močový katetr, který je třeba před vyšetřením ledvinového graftu uzavřít. V opačném případě by došlo k odtoku moči do sběrného sáčku a neviděli bychom plnění močového měchýře radiofarmakem. Během studie průběžně sledujeme, zda nedochází k retenci v dutém systému transplantované ledviny.
První vyšetření u pacienta s transplantovanou ledvinou je vhodné provést do 24 hodin po transplantaci, protože lze pak odlišit akutní rejekci, která nastupuje později, od ostatních komplikací. Nejlépe se osvědčuje série opakovaných vyšetření v různých časových odstupech: den–týden–měsíc a dle další potřeby.
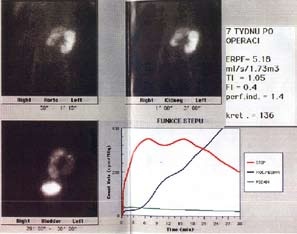
Vyhodnocování studie. Studie je hodnocena:
a) vizuálně, kdy se posuzuje kontrast a homogenita transplantované ledviny, kontury ledviny, ložiskové změny a plnění močového měchýře;
b) kvanti- tativně matematickým výpočtem ERPF (efektivní průtok plazmy ledvinou);
c) hodnocení nefrogramu, na kterém se sleduje strmost funkčního segmentu a následný pokles křivek ve třetí fázi.
Nejčastější pooperační komplikace
ATN (akutní tubulární nekróza) – je způsobena především ischemizací ledviny v období od vynětí štěpu od dárce do okamžiku obnovení průtoku krve ledvinou při transplantaci. Vzniká častěji u kadaverózních dárců. Pro ATN je charakteristická dobrá perfúze graftu, přetrvávající retence v parenchymu a malá nebo zcela chybějící exkrece do dutého systému. Na scintigrafických snímcích pozorujeme chybění radioaktivity v močovém měchýři.
Rejekce:
a) hyperakutní rejekce se vyskytuje vzácně a vzniká do 24 hodin po transplantaci, není proto popisovanou metodou zachytitelná;
b) akutní rejekce vzniká většinou za 4–5 dní po transplantaci, dochází ke snížení perfúze a akumulace radiofarmaka v ledvině. Je nutné vyloučit zejména odtokovou obstrukci;
c) chronická rejekce vzniká pozvolna, dochází k pomalému ireverzibilnímu procesu, k poklesu perfúze, funkce a exkrece, který vede zpravidla ke ztrátě funkce štěpu.
Cévní komplikace:
a) trombóza renální arterie – dochází k aperfúzi štěpu;
b) stenóza arteria renalis – vzniká pozvolna a dochází k renovaskulární hypertenzi;
c) infarkt ledviny – způsobí aperfúzi graftu.
Chirurgické komplikace:
zánět; infekce rány; absces; hematom; urinom (únik moči do peritoneální dutiny) – typické pro urinom je difúzní hromadění radiofarmaka mimo štěp, uretery a močový měchýř; obstrukce ureteru – může vzniknout kdykoli. Pracují-li ještě i autologní ledviny, může se objevovat moč v močovém měchýři.
Závěr
Vedle ostatních zobrazovacích metod (USG, CT, NMR, angiografie, IVU) napomáhá scintigrafie graftu v diagnostice a léčbě pooperačních komplikací. Jedním z hlavních problémů současné transplantační medicíny je nedostatek orgánů k transplantacím. Transplantaci lze provést výhradně osobě zařazené v čekací listině (Národní registr osob čekajících na transplantaci, tzv. waiting list). Tato čekací listina je seznam všech možných příjemců, kteří mají selhání ledvin a jsou v daný okamžik schopni transplantaci podstoupit. Při dárcovství ledvin rozlišujeme dárce kadaverózního (zemřelého) a žijícího. Jednoznačným řešením, jak zvýšit dostupnost transplantací ledvin nemocným s chronickým selháváním ledvin, je transplantace ledvin od žijícího dárce (příbuzenská transplantace). Přijmout darovanou ledvinu je pro příjemce velmi povzbudivé a výhodné z několika důvodů. Především jde o zkrácení doby čekání na transplantaci, zkrácení hemodialyzační léčby na minimum, prodloužení funkce transplantované ledviny, opomenout nelze ani příznivý psychologický dopad příbuzenské transplantace ledvin. V porovnání s dialyzační léčbou zdvojnásobuje předpokládanou dobu přežití. Ke zvýšení počtu žijících dárců by napomohla lepší informovanost lékařů a pacientů o této metodě léčby. Hlavním důvodem je změna organizace transplantačního a odběrového programu, a proto je věnováno velké úsili dárcovskému programu, což je celý soubor informací o možnosti darování orgánů, vyšetření jak dárce, tak příjemce, dodržení právních úkonů apod. Informace o potenciálních dárcích z regionálních zdravotnických zařízení přijímají koordinátoři transplantačních center (TC), kteří mají nepřetržitou službu. Dalším faktorem vedoucím ke zvýšení počtu dárců orgánů je rozšíření indikačních kritérií. Není již limitován například věk dárce, rovněž anamnézy některých onemocnění nemusí být kontraindikací k dárcovství. Z medicínského hlediska je to nasazení co nejvhodnější léčby imunosupresivy, eliminace či snížení komplikací a nežádoucích účinků imunosupresivní terapie, správná indikace k zařazení nemocných do čekací listiny (waiting list) Národního registru osob čekajících na transplantaci s cílem co nejdelšího přežívání nemocných po transplantacích a co nejvyšší kvality jejich života.
Kazuistika
Pacientka, 75 let, byla od roku 2004 sledována pro glomerulonefritidu, cysty ledvin a oboustrannou nefrolitiázu. Z důvodů diabetické nefropatie s renální insuficiencí je přistoupeno k transplantaci ledviny. Z osobní anamnézy je uváděno, že se 15 let léčí na hypertenzi, 6 let má diagnostikován DM (diabetes mellitus) 2. typu (na dietě a inzulinu). Projevuje se u ní sekundární anémie. V roce 2005 prodělala AIM (akutní infarkt myokardu) a akutně byla provedena PTCA (perkutánní transluminální koronární angioplastika) na RIA (ramus interventricularis anterior) s 2 stenty a zároveň došlo i k náhradě aortální chlopně. Po operaci byla ponechána trvalá antikoagulační léčba.
11. 8. 2006 byla provedena transplantace kadaverózní ledviny, která byla uložena do levého retroperitonea.
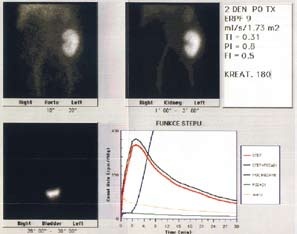
15. 8. 2006 bylo provedeno první scintigrafické vyšetření transplantované ledviny. Lékař popsal dobrou perfúzi graftu a tubulární funkci, tranzit parenchymem do vývodných močových cest byl zpomalený nejspíše v důsledku ATN (akutní tubulární nekróza). Nepozoroval retenci v kalichopánvičkovém systému štěpu.
17. 8. 2006 byla provedena chirurgická revize pro hematom v dutině břišní. Průběh hospitalizace byl komplikován pozdním nástupem funkce štěpu. Hodnota kreatininu v séru se nyní pohybovala kolem 760 μmol/l, a proto byla opakovaně nutná hemodialýza.
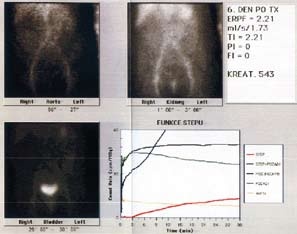
28. 8. 2006 klinik požadoval další vyšetření scintigrafie graftu. Perfúze štěpu byla dobrá, funkce nezlepšena, močový měchýř se vůbec nezobrazil. Pravděpodobně šlo o těžší průběh akutní tubulární nekrózy s vedlejším nálezem hematomu v dutině břišní. Stav se postupně upravil.
7. 9. 2006 proběhla kontrolní scintigrafie graftu. Došlo ke zlepšení perfúze funkce štěpu.
13. 2. 2007 byla pacientka přijata na transplantační jednotku intenzivní péče pro makroskopickou hematurii. Laboratorně byl stanoven kreatinin v séru 141 μmol/l. Byla potvrzena hydronefróza graftu se suspektním urinomem a pacientka musela podstoupit punkci. Pokus o zavedení hydrofilního vodiče byl však neúspěšný a byla indikována další scintigrafie graftu.
23. 2. 2007 scintigrafie štěpu potvrdila dobrou perfúzi i funkci. Plnění močového měchýře se zobrazovalo opožděně a kolem něj byla ložiska depozity radioaktivity. Z tohoto důvodu lékař doporučil využít ještě jinou zobrazovací metodu, protože se domníval, že může jít o urinom.
3. 5. 2007 pacientka byla přijata na transplantační jednotku intenzivní péče pro zhoršení funkce graftu a pro indikování urinomu, byla provedena dočasná nefrostomie a reoperace urinomu s reinplantací ureteru graftu a stent. Průběh však byl komplikován uroinfekcí a pacientka musela být přeléčena antibiotiky (ATB).
4. 5. 2007 byla provedena scintigrafie graftu, kdy lékař popsal globální sníženou funkci, dobrou perfúzi štěpu a retenci v dutém systému graftu. V závěru studie se objevila depozice radiofarmaka ve spodním pólu graftu, odpovídající urinomu.
27. 11. 2008 – další hospitalizace pro podezření na uroinfekt, febrilie po dobrání ATB, zimnice, třesavka, teplota přes 38 °C. Kreatinin v séru je 200 μmol/l. Po přeléčení antibiotiky došlo k poklesu CRP (C-reaktivní protein) a pacientka byla propuštěna do domácí péče.
13. 3. 2009 byla opět přijata na transplantační jednotku intenzivní péče pro dušnost, febrilie s třesavkou, krvácení z nosu a tmavou moč. Došlo k renální insuficienci a k selhání funkce štěpu. Další průběh komplikoval rozvoj mykotické infekce se sekundárním septickým stavem.
31. 3. 2009 byla doporučena celotělová scintigrafie pro suspektní zánětlivý proces, vyšetření však ložiskový zánětlivý proces neprokázalo. Stav se po ATB opět postupně upravil a pacientka byla propuštěna do domácí péče. Nyní pravidelně dochází ke kontrolním vyšetřením na interní a nefrologickou ambulanci.
Z uvedených zkušeností vyplývá, že dynamická scintigrafie transplantovaného štěpu je velmi užitečnou metodou pro nemocné po operaci a pro jejich pooperační monitorování.
Drahoslava Nováková, Klinika nukleární medicíny FN Ostrava
Recenzovaly:
Mgr. Ludmila Klemsová, vrchní sestra kardiovaskulárního oddělení, FN Ostrava
MUDr. Jarmila Dědochová, Interní klinika, nefrologická a transplantační ambulance, FN Ostrava
Literatura:
1. Sharp PF et al. Practical nuclear medicine. London: Birkhäuser 2005, 185233875X.
2. Adamec M, Janoušek L. Historie transplantací nitrobřišních orgánů v IKEM Praha z pohledu chirurga. Folia Gastroenterol Hepatol 2005; 3 (Suppl 1): S8–S12.
3. Třeška V a kol. Transplantologie pro mediky. Praha: Karolinum 2002, 80-246-0331-4.
Další články v tomto čísle
- Dignitatis memores, ad optima intenti
- Rozhovor s Lenkou Hejzlarovou: Tah na bránu Komory
- Rouškovací systémy a ochranné oděvy na operačních sálech
- Vhodný výběr rukavic – vinyl, latex, nebo nitril?
- Z praxe zkušené stomasestry (II. díl)
- ANTT : standardní přístup k aseptické technice
- Je mytí rukou taková věda?
- Využití canisterapie v ošetřovatelském procesu
- Tkáňová lepidla k uzavírání chirurgických incizí
- Zavádění a udržování kvality a bezpečí zdravotní péče v zařízeních nemocničního typu na území ČR











