


Číslo 5 / 2025
Časová úspora při použití IC-EKG pro potvrzení umístění distálního konce PICC katétru ve srovnání s rentgenem hrudníku
Souhrn: Cíl: Stále větší pozornost si získávají periferně zavedené centrální žilní katétry (PICC) s využitím metody intrakavitárního elektrokardiogramu (IC-EKG). Cílem této studie bylo podpořit a přidat další důkazy o proveditelnosti, časové úspoře, přesnosti, bezpečnosti umístění distálního konce katétru pomocí IC-EKG ve srovnání s rentgenem (RTG) hrudníku, eliminovat zbytečné ozařování a další vyšetřování pacienta. Tato studie byla provedena sestrami PICC týmu a jedná se o první ošetřovatelskou studii v České republice na toto téma. Metody: Monocentrická, prospektivní, nerandomizovaná klinická studie. Data byla sbírána ve FN Ostrava od června 2020 do ledna 2023. Primárním cílem bylo měření času, který uplynul mezi IC-EKG a popisem RTG hrudníku, sekundárním cílem bylo měření úspěšnosti pomocí IC-EKG ve shodě s RTG hrudníku dle nastavených kritérií a potvrzení distálního konce katétru v kavoatriální junkci (CAJ). Výsledky: Byla analyzována data 453 po sobě jdoucích pacientů, kteří podstoupili zavedení PICC. Primární data ukázala, že minimální doba mezi IC-EKG a popisem RTG hrudníku lékařem byla 1 min a maximální doba byla 400 min, medián čekací doby 80 min. Sekundární data ukázala úspěšnost IC-EKG ve shodě s RTG hrudníku dle nastavených kritérií u 84,8 % (n = 384) pacientů. Závěr: Metodu IC-EKG mohou sesterské týmy zabývající se cévními vstupy používat bezpečně a efektivně bez rizika komplikací. Ukázalo se, že jde o spolehlivou metodu potvrzení uložení distálního konce katétru umožňující použití PICC ihned po zavedení bez prodlevy v léčbě pacienta.
Klíčová slova: časová úspora, rentgen hrudníku, centrální žilní katétr, distální konec katétru, intrakavitární elektrokardiogram
Time savings when using IC-ECG navigation to confirm the PICC tip location compare to chest X-ray
Summary: Aim: Peripherally inserted central catheters (PICCs) with the use of intracavitary electrocardiogram (IC-ECG) method are gaining more and more attention. The aim of this study was to support and add more evidence about feasibility, accuracy and safety of IC-ECG tip location comparing to a chest X-ray in order to eliminate unnecessary radiation and additional patient’s investigation. This study was performed by nurses led PICC team and it is the first nursing study in Czech Republic on this topic. Methods: A single center, prospective, non-randomized clinical study. Data were collected over 3 years at University Hospital Ostrava, Czech Republic, from June 2020 to January 2023. The primary outcome was measurement of time elapsed between IC-ECG and chest X-ray confirmation, secondary outcome measured success rate using IC-ECG and confirming the tip of the catheter in cavo-atrial junction (CAJ). Results: Data of 453 consecutive patients who underwent PICC insertion were analysed. The primary outcome showed the minimum time elapsed between IC-ECG and chest X-ray confirmation by physician was 1 min and the maximum time was 400 min, with the median waiting time of 80 min. Secondary outcome showed IC-ECG success rate in 84.8% (N = 384) of the sample. Conclusion: IC-ECG confirmation method can be used by nursing teams safely and effectivelly without a risk for complications. It proved to be reliable method of confirming the tip of the catheter and allowing the use of PICC immediately post insertion without a delay in patient’s treatment.
Key words: peripherally inserted central catheter, chest X-ray, PICC tip navigation, catheter tip location, intracavitary electrocardiogram
doi: 10.48095/ccflo2025152
Úvod
Periferně zavedený centrální katétr (PICC) se stal nezbytnou součástí střednědobé a dlouhodobé intravenózní terapie v současné péči o pacienty (Barton, 2016; Charvát et al., 2016; Shen et al., 2022). Léky zvažované pro střednědobou nebo dlouhodobou intravenózní terapii jsou obvykle s nízkým nebo vysokým pH a vysokou osmolaritou, což má za následek poškození endotelu cév, a proto musí být podávány do centrální žíly: např. intravenózní antibiotika, parenterální výživa, chemoterapie a další iritující látky (Charvát et al., 2016; Bloemen et al., 2018; Moureau, 2019; Xiao et al., 2020; Pittiruti et al., 2021; Shen et al., 2022). Kromě toho se PICC využívá i při odběru krve a v neposlední řadě je jedinou možností přístupu pro pacienty s vyčerpaným periferním žilním systémem (Moureau, 2019; Mack et al., 2020). Aby bylo možné bezpečně podat tyto intravenózní léky a předejít jakýmkoli komplikacím, je důležité, aby distální konec PICC katétru byl ve správné poloze (La Greca, 2014; Pittiruti et al., 2020; Chai et al., 2021). Mezi komplikace související s nesprávným uložením distálního konce patří srdeční arytmie, srdeční tamponáda, poškození katétru, trombóza, infekce a dokonce úmrtí (Bloemen et al., 2018; Mack et al., 2020; Erskine et al., 2021). Komplikace jsou nežádoucí události, které oddalují léčbu pacienta a zvyšují náklady zdravotnického zařízení (Erskine et al., 2021). Správná poloha distálního konce katétru je proto důležitá a nachází se na přechodu horní duté žíly do pravé síně. Toto místo je označováno jako kavoatriální spojení (CAJ) (Chan et al., 2016; Elli et al., 2017; Yu et al., 2019; Liu et al., 2022). IC-EKG metoda byla používána zejména lékaři u dospělých pacientů, u pacientů s renálním onemocněním i u pediatrické populace (Pittiruti et al., 2020; Xiao et al., 2020; Liu et al., 2022). Existuje pouze několik studií týkajících se použití IC-EKG metody nelékařským zdravotnickým personálem (sestrami), ale žádná z České republiky (Moureau et al., 2010; Barton, 2016; Bidgood, 2016). IC-EKG dokazuje svou účinnost, vysokou míru přesnosti, potvrzení v reálném čase, nákladovou efektivitu, širokou použitelnost, což je výhodnější oproti RTG hrudníku (Bloemen et al., 2018; Pittiruti et al., 2018; Liu et al., 2022). Technika IC-EKG je podporována mezinárodními společnostmi, jako je Infusion Nurses Society (INS) nebo Italská společnost pro žilní přístup (GAVeCeLT), která navrhla i protokol pro bezpečné zavedení PICC (protokol SIP) (Gorski et al., 2021; Brescia et al., 2022). Evropská společnost pro parenterální výživu (ESPEN) byla dokonce první společností, která v roce 2009 doporučila použití IC-EKG pro ověření polohy distálního konce katétru (ESPEN, 2009; Pittiruti et al., 2020). Metoda IC-EKG je mezi odborníky známá a používaná, přesto je v České republice adaptována nejednotně. V posledních letech si však IC-EKG metoda ověřovaní u zavedení PICC, ale i jiných žilních katétrů získává stále větší pozornost. V této studii jsme se primárně zaměřili na měření času v minutách mezi umístěním distálního konce katétru pomocí IC-EKG a RTG hrudníku a mezi IC-EKG a potvrzením RTG hrudníku. Dále jsme zahrnuli dobu, která uplynula mezi RTG hrudníku a popisem RTG hrudníku lékařem. Jak je známo, čekání na rentgen hrudníku a na jeho popis oddaluje léčbu pacienta a první použití PICC. Sekundárním cílem bylo vyhodnotit úspěšnost IC-EKG metody. To je založeno na skutečnosti, že metoda IC-EKG je bezpečná a proveditelná. Na základě těchto výsledků sesterský PICC tým ve FN Ostrava implementuje IC-EKG jako primární metodu ověření distálního konce PICC katétru do klinické praxe.
Metody
Design studie a výběr účastníků
Z přehledu literatury vyplynulo, že určení pozice konce centrálního žilního katétru pomocí IC-EKG je technicky možné a úspěšné (Hoffman et al., 1988; Pittiruti et al., 2008; Moureau et al., 2010; Barton, 2016; Bloemen et al., 2018; Yu et al., 2019; Mack et al., 2020; Xiao et al., 2020; Brescia et al., 2022; Liu et al., 2022). Moureau byla považována za sestru-průkopnici v USA, která provedla studii na metodu IC-EKG u zavedení PICC (Moureau et al., 2010). Byla následována studií Bartona a Bidgooda, obě tyto studie byly publikovány v British Journal of Nursing v roce 2016. Sesterské studie na toto téma nejsou časté, což nás přivedlo k myšlence provést sesterskou studii na IC-EKG s PICC v České republice. V roce 2020 FN Ostrava stále potvrzovala pozici distálního konce PICC pomocí RTG, což jsme chtěli změnit.
Tato studie je monocentrická, prospektivní, nerandomizovaná a intervenční. Data byla sbírána a analyzována po dobu 3 let ve FN Ostrava od června 2020 do ledna 2023. Kritériem pro zařazení bylo min. 18 let, indikace pro střednědobý nebo dlouhodobý přístup a podepsaný informovaný souhlas. Ze studie byli vyloučeni onkologičtí pacienti, děti a ti, kteří s výkonem nesouhlasili.
Populace a sběr dat
Studijní vzorek tvořilo 453 účastníků splňujících kritéria pro zařazení, všichni měli obě metody potvrzení distálního konce PICC katétru. U každého účastníka byl zjišťován věk, pohlaví, pracoviště, diagnóza, důvod zavedení, konfirmační metody IC-EKG a RTG hrudníku. Data byla shromažďována elektronicky proškolenou a kompetentní sestrou PICC týmu.
Postup pro umístění distálního konce katétru
PICC katétry byly zavedeny pomocí osmi kroků SIP protokolu u všech účastníků dvěma sestrami, které absolvovaly certifikovaný kurz zavádění PICC. Výkon byl u lůžka nebo na intervenčním sále. Po zavedení PICC byl distální konec katétru lokalizován pomocí IC-EKG s použitím třísvodového EKG TLS Pilot Vygon. Byl získán a uložen předprocedurální EKG. Když byl PICC zaveden a trhací sheath stále na místě, připojili jsme k vodicímu drátu v PICC sterilní aligátorový kabel od firmy Vygon (Combcard). Pak byla sledována P vlna na přístroji TLS Pilot Vygon. Když P vlna dosáhla nejvyšší amplitudy, distální konec katétru byl v CAJ. Jinými slovy, P vlna byla pozitivní ve stejné úrovni jako QRS komplex. Přístroj TLS Pilot umožňoval automatické potvrzení, když byla P vlna v nejvyšší amplitudě, na obrazovce se objevila zelená čára. Poté jsme navedli PICC hlouběji, dokud nebyl před P vlnou viditelný negativní segment, což znamenalo, že se distální konec nachází v pravé srdeční síni. Tuto techniku jsme použili ke kontrole, zda katétr sledoval správný směr k srdci. V dalším kroku byl katétr vytažen zpět do CAJ. EKG záznam byl uložen elektronicky a pacient byl odeslán k RTG hrudníku. V případech, kdy IC-EKG nešel hodnotit, byl pacientovi proveden pouze RTG hrudníku. U všech 453 účastníků byl pořízen postprocedurální RTG hrudníku, který byl zkontrolován kompetentní PICC sestrou, lékařem pracujícím s PICC týmem a také radiologem.
Definice IC-EKG a CAJ, RTG hrudníku a CAJ
V době návrhu studie jsme použili následující kritéria/definici správné výšky P vlny. Správné potvrzení IC-EKG bylo určeno P vlnou, kdy maximální amplituda P vlny dosahovala maxima QRS (Moureau et al., 2010). Přístroj TLS Pilot Vygon navíc poskytl automatické potvrzení maximální amplitudy P vlny. Předpokládá se, že maximální P vlna odpovídá anatomickému umístění CAJ (Jeon et al., 2006; Johnston et al., 2014). Jiní autoři použili různé strategie, jak zmiňují Liu et al. (2022) ve své studii, např. použili mezník pro P vlnu 50–80 % QRS komplexu. Bez ohledu na základní rytmy jsme se pokusili o IC-EKG u všech účastníků. Nemožnost získat maximální výšky P vlny IC-EKG nebo nemít vůbec změny P vln byly shromážděny a zdokumentovány ve zdravotní dokumentaci pacienta. RTG hrudníku byl prováděn na radiologickém oddělení nebo u lůžka v PA (posterior anterior) nebo AP (anterior posterior) pozici. Správné umístění PICC na RTG hrudníku bylo definováno jako umístění distálního konce katétru pod karinou v CAJ. Použili jsme Johnstonovu et al. rentgenovou definici hrudníku, kde je CAJ definována jako dvě obratlová těla pod dolním okrajem kariny vč. obratlových plotének (Johnston et al., 2014). Malpozice na RTG hrudníku byla definována jako špička nad karinou – příliš vysoko (katétr byl krátký) nebo hluboko v pravé síni (katétr byl příliš dlouhý) (Johnston et al., 2014).
Statistická analýza
Číselné proměnné jsou popsány mediány, mezikvartilovými rozsahy (dolní a horní kvartily) a rozsahy (minima a maxima) a jsou vizualizovány pomocí boxplotů. Kategorické proměnné jsou reprezentovány jako absolutní četnosti a relativní četnosti (%). Hladina významnosti byla nastavena na 0,05 a veškerá statistická analýza byla provedena v softwaru R (verze 4.2.1).
Etické aspekty
Tato studie byla schválena Institucionální etickou komisí FN Ostrava. Číslo schválení: 383/2020 a Helsinská deklarace z roku 1964. Účastníkům byl vysvětlen účel této studie a důvod IC-EKG a RTG hrudníku po zavedení PICC. Od všech účastníků byl získán písemný informovaný souhlas. Účastníci byli ujištěni, že mohou ze studie odstoupit a jejich údaje budou anonymizovány a budou důvěrné.
Výsledky
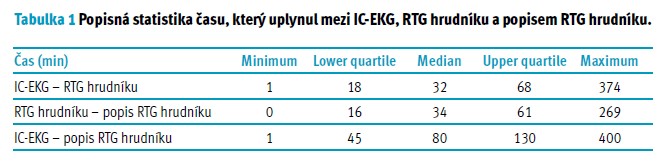
Celkem bylo do studie zařazeno 453 pacientů, z toho 199 žen (43,9 %) a 254 mužů (56,1 %). Medián věku všech pacientů byl 67 let (interquartile range (IQR): 56–75 let, rozmezí: 18–95 let). Primárním cílem bylo měření časových intervalů. Medián času, který uplynul mezi IC-EKG a RTG hrudníku, byl 32 min (IQR: 18–68 min), minimální uplynulý čas byl 1 min a maximální uplynulý čas byl 374 min. To znamená, že polovina pacientů musela čekat déle než 32 min a 25 % pacientů muselo čekat na RTG hrudníku déle než 68 min.
Medián doby, která uplynula mezi RTG hrudníku a popisem RTG hrudníku lékařem pro použití PICC, byl 34 min (IQR: 16–61 min), minimální uplynulý čas byl 0 min a maximální uplynulý čas byl 269 min.
Medián doby, která uplynula mezi IC-EKG a popsáním RTG hrudníku lékařem byl 80 min (IQR: 45–130 min), minimální uplynulý čas byl 1 min a maximální uplynulý čas byl 400 min. To znamená, že 75 % pacientů muselo čekat na schválení k použití PICC více než 45 min od IC-EKG navigace (obr. 1, tab. 1).
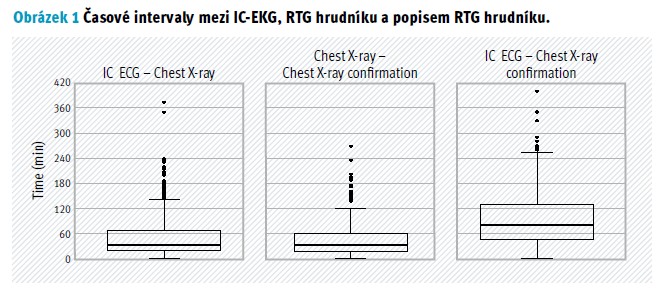
Jako druhotný cíl byla sledována míra úspěšnosti IC-EKG a analyzovala se jen data, kdy byla shoda IC-EKG a RTG hrudníku dle nastavených kritérii této studie. Ze 453 pacientů byl IC-EKG úspěšný a souhlasil s RTG hrudníku, dle dané definice, u 384 pacientů (84,8 %, 95% confidence interval (CI): 81,1–88,0 %). Pokud by úspěšné IC-EKG bylo přímou indikací k použití PICC, PICC se okamžitě mohl použít u 384 pacientů (84,8 %). Prodloužená čekací doba pacientů na potvrzení RTG hrudníku (medián: 80 min; IQR: 45–130 min) by mohla být eliminována. To znamená, že u 75 % pacientů se mohl PICC použít alespoň o 45 min dříve.
Diskuze
Primární šetření v naší studii souviselo s časovou prodlevou mezi IC-EKG a RTG hrudníku v různých situacích (tab. 1). Historicky byl rentgen považován za zlatý standard pro potvrzení správné pozice distálního konce žilního katétru (Moureau et al., 2010; La Greca 2014; Gao et al., 2018; Yu et al., 2019; Ren et al., 2021). Metoda vyžaduje laboranta provádějícího RTG vyšetření a lékaře, který snímek popíše. V naší studii jsme zkoumali, jak velké časové zpoždění nastane, než se PICC může použít. Za prvé, medián doby, která uplynula mezi IC-EKG a provedením RTG hrudníku, byl 32 min. Minimální uplynulý čas byl 1 min a maximální uplynulý čas byl 374 min. To znamená, že polovina pacientů musela čekat déle než 32 min a 25 % pacientů muselo čekat na RTG hrudníku déle než 68 min. Doba 1 min byla hlášena pouze u jednoho pacienta, kde byl radiologický laborant přítomen u lůžka. Za druhé, medián času, který uplynul mezi rentgenem hrudníku a popsáním snímku hrudníku lékařem, byl 34 min (IQR: 16–61 min). Minimální uplynulý čas byl 0 min a maximální uplynulý čas byl 269 min. Žádná časová prodleva (0 min) byla u jednoho pacienta, kdy byl u výkonu radiolog, který RTG ihned popsal. Za třetí, a to je nejdůležitější, jsme zjišťovali dobu mezi provedeným IC-EKG a popisem RTG hrudníku lékařem, zde se jednalo o nejdelší prodlevu. Minimální čas byl 1 min, maximum bylo 400 min s mediánem zpoždění 80 min. Tři čtvrtiny (75 %) pacientů čekaly na popis RTG hrudníku před použitím PICC déle než 45 min. V literatuře byly nalezeny podobné výsledky, ale pouze pro RTG hrudníku a popis RTG hrudníku ve studii Olivera a Jonese (2016). Autoři uváděli minimální čas 0 min a nejdelší časové zpoždění 5 hod 5 min (305 min) s průměrným časovým zpožděním 1 hod 33 min (93 min) (Oliver et al., 2016).
Další časová měření jako v naší studii ještě nebyla zkoumána, proto nejsou k dispozici žádná data, se kterými bychom mohli porovnávat, ale rozhodně nám ukazují prodlevu v péči o pacienty. U druhého výsledku od června 2020 do ledna 2023 v naší monocentrické intervenční studii 384 ze 453 pacientů podstoupilo úspěšné zavedení PICC s IC-EKG a současným potvrzením RTG hrudníku. Úspěšnost k okamžitému použití je 84,8 %. To je méně než ve studii Moureau et al. (2010), kde shoda dosáhla 97 %, ale s menším počtem účastníků. Moureau et al. (2010) provedli jednu z prvních ošetřovatelských studií, která prokázala, že IC-EKG je spolehlivou metodou potvrzení distálního konce PICC u pacientů bez abnormalit srdečního rytmu nebo cév v režii kompetentního a stabilního týmu. Na toto téma nebyly nalezeny žádné české studie. Další studie, zejména z Číny a Itálie, související s PICC také prokázaly, že navádění katétru a potvrzení distálního konce katétru pomocí IC-EKG je spolehlivou metodou, jejich výsledky kolísají mezi 89 a 99 % (Yuan et al., 2017; Liu et al., 2019; Yu et al., 2019). V randomizované multicentrické studii zahrnující 2 250 dospělých pacientů byla zjištěna úspěšnost 99,3 % (Yin et al., 2019). Ve stejném roce 2019 metaanalýza 5 randomizovaných studií, 2 italských a 3 čínských, které zahrnovaly celkem 1 672 pacientů, odhalila, že přesné umístění distálního konce PICC bylo v 89,7 % (Liu et al., 2019). Tyto výsledky jsou velmi podobné těm v naší studii. O těchto studiích však nemůžeme říci, že byly prováděny výhradně nelékařskými pracovníky.
Údaje z předchozích studií nepotvrzují výskyt komplikací u IC-EKG (Moureau et al., 2010; Pitturuti et al., 2012; Zhou et al., 2017; Liu et al., 2019; Yu et al., 2019). Systém IC-EKG je výkonný nástroj, který zvyšuje produktivitu při zavádění, odlehčuje radiologickým oddělením (Gullo et al., 2022) a je potvrzeno, že je ekonomicky efektivní (Pittiruti et al., 2011). Použití RTG hrudníku naopak vystavuje pacienta zbytečnému záření, pacient podstupuje další zákrok a/nebo transport a doba do použití PICC se prodlužuje (Bloemen et al., 2018).
U 69 pacientů, u kterých nebylo dosaženo potvrzení pomocí IC-EKG ve shodě s RTG hrudníku dle nastavených kritérií, byly zjištěny srdeční arytmie, malpozice, distální konec nad nebo pod úrovní CAJ. Během doby studie mělo 35 z 69 pacientů fibrilaci síní. Fibrilace síní byla nevýhodou, v podstatě omezením pro potvrzení IC-EKG. Tyto pacienty jsme z naší studie nevyloučili, protože jsme nestanovili meze měření, abychom je zahrnuli, jak je zdokumentováno ve studii Gao et al., kteří zkoumali pacienty s fibrilací síní a změnou f vlny. Fibrilační vlny ≥ 0,5 cm brali jako správné uložení distálního konce katétru. Jejich výsledky byly uspokojivé a doporučují IC-EKG pro tuto skupinu pacientů (Gao et al., 2018). U 3 pacientů jsme měli stimulační rytmus, u 2 junkční rytmus, u 18 malpozici (8× stočený, 2× kontralaterální, 4× nedosáhl CAJ, 2× nezaveden, 2× centrální žilní katétr bránící v IC-EKG), u 8 pacientů jsme měli katétr těsně pod CAJ 1 až 2 cm a 3 měli distální konec 2 cm nad CAJ, tedy mimo určenou definici CAJ naší studie.
Limitace studie
Jedná se o nerandomizovanou studii. Další limitací je, že nebyla brána v úvahu poloha pacienta při RTG hrudníku, která by mohla mít vliv na pozici distálního konce katétru. Budoucí studie by mohly být randomizované, multicentrické, vč. skupiny pacientů s fibrilací síní, a také by mohly zahrnovat ekonomickou stránku IC-EKG metody.
Závěr
Naše studie ukázala, že určení pozice konce PICC s použitím IC-EKG metody certifikovanou sestrou je přesné a efektivní. Při srovnání s prováděním rentgenového snímku hrudníku výrazně zkracuje čas potřebný k potvrzení jeho správné pozice a nezatěžuje pacienta rentgenovým zářením.
Literatura
1. BARTON A. Confirming PICC tip position during insertion with real-time information. Br J Nurs 2016; 25(2): S17–S21. doi: 10.12968/bjon.2016.25.Sup2.S17.
2. BIDGOOD C. Improving the patient experience with real-time PICC placement confirmation. Br J Nurs 2016; 25(10): 539–543. doi: 10.12968/bjon.2016.25.10.539.
3. BLOEMEN A., DANIELS A. M., SAMYN M. G. et al. Electrocardiographic-guided tip positioning technique for peripherally inserted central catheters in a Dutch teaching hospital: Feasibility and cost-effectiveness analysis in a prospective cohort study. J Vasc Access 2018; 19(6): 578–584. doi: 10.1177/1129729818764051.
4. BRESCIA F., PITTIRUTI M., SPENCER T. R. et al. The SIP protocol update: Eight strategies, incorporating Rapid Peripheral Vein Assessment (RaPeVA), to minimize complications associated with peripherally inserted central catheter insertion. J Vasc Access 2022; 25(1): 5–13. doi: 10.1177/11297298221099838.
5. ELLI S., ABBRUZZESE C., CANNIZZO L. et al. “Extended subcutaneous route” technique: a quick subcutaneous tunnelling technique for PICC insertion. J Vasc Access 2017; 18(3): 269–272. doi: 10.5301/jva.5000647.
6. ERSKINE B., BRADLEY P., JOSEPH T. et al. Comparing the accuracy and complications of peripherally inserted central catheter (PICC) placement using fluoroscopic and the blind pushing technique. J Med Radiat Sci 2021; 68(4): 349–355. doi: 10.1002/jmrs.533.
7. GAO Y., LIU Y., ZHANG H. et al. The safety and accuracy of ECG-guided PICC tip position verification applied in patients with atrial fibrillation. Ther Clin Risk Manag 2018; 14: 1075–1081. doi: 10.2147/TCRM.S156468.
8. GORSKI L. A., HADAWAY L., HAGLE M. E. et al. Infusion therapy standards of practice, 8th Edition. J Infus Nurs 2021; 44(1S): S1–S224. doi: 10.1097/NAN.0000000000000396.
9. GULLO G., QANADLI S. D. ECG-based techniques to optimize peripherally inserted central catheters: rationale for tip positioning and practical use. Front Cardiovasc Med 2022; 9: 765935. doi: 10.3389/fcvm.2022.765935.
10. HOFFMAN M. A., LANGER J. C., PEARL R. H. et al. Central venous catheter – no X-rays needed: a prospective study in 50 consecutive infants and children. J Pediatr Surg 1988; 23(12): 1201–1203. doi: 10.1016/s0022-3468(88)80344-0.
11. CHAI Y. H., HAN S. Y., ZHU Y. X. et al. Electrocardiographic localization of peripherally inserted central catheter tip position in critically ill patients with advanced cancer: an application study. Ann Noninvasive Electrocardiol 2022; 27(2): e12918. doi: 10.1111/anec.12918.
12. CHARVÁT J., FRICOVÁ J., CHOVANEC V. et al. Žilní vstupy: dlouhodobé a střednědobé. Praha: Grada Publishing 2016.
13. CHAN T. Y., ENGLAND A., MEREDITH S. M. et al. Radiologist variability in assessing the position of the cavoatrial junction on chest radiographs. Br J Radiol 2016; 89(1065): 20150965. doi: 10.1259/bjr.20150965.
14. JEON Y., RYU H. G., YOON S. Z. et al. Transesophageal echocardiographic evaluation of ECG-guided central venous catheter placement. Can J Anaesth 2006; 53(10): 978–983. doi: 10.1007/BF03022525.
15. JOHNSTON A. J., HOLDER A., BISHOP S. M. et al. Evaluation of the Sherlock 3CG Tip Confirmation System on peripherally inserted central catheter malposition rates. Anaesthesia 2014; 69(12): 1322–1330. doi: 10.1111/anae.12785.
16. LA GRECA A. Evaluation techniques of the PICC tip placement. In: SANDRUCCI S., MUSSA B. (eds.). Peripherally inserted central venous catheters. Milano: Springer 2014: 63–83.
17. LIU G., HOU W., ZHOU C. et al. Meta-analysis of intracavitary electrocardiogram guidance for peripherally inserted central catheter placement. J Vasc Access 2019; 20(6): 577–582. doi: 10.1177/1129729819826028.
18. LIU B., LIU Y., LI J. et al. A feasible and safe standardized protocol for ultrasound and intracavitary electrocardiogram-based tip navigation and tip location during placement of peripherally inserted central catheters. J Vasc Access 2024; 25(3): 935–642. doi: 10.1177/11297298221095039.
19. MACK V., NIßLER D., KASIKCI D. et al. Magnetic tracking and electrocardiography-guided tip confirmation system versus fluoroscopy for placement of peripherally inserted central catheters: a randomized, noninferiority comparison. Cardiovasc Intervent Radiol 2020; 43(12): 1891–1897. doi: 10.1007/s00270-020-02551-0.
20. MOUREAU N. L., DENNIS G. L., AMES E. et al. Electrocardiogram (EKG) guided peripherally inserted central catheter placement and tip position: results of a trial to replace radiological confirmation. JAVA 2010; 15(1): 8–14. doi: 10.2309/java.15-1-3.
21. MOUREAU N. L. Vessel Health and Preservation: The Right Approach for Vascular Access. Spring Open. Cham: Springer 2019.
22. OLIVER G., JONES M. ECG-based PICC tip verification system: an evaluation 5 years on. Br J Nurs 2016; 25(19): S4–S10. doi: 10.12968/bjon.2016.25.19.S4.
23. PITTIRUTI M., SCOPPETTUOLO G., LA GRECA A. et al. The EKG method for positioning the tips of PICCs: results from two preliminary studies. JAVA 2008; 13(4): 179–186. doi: 10.2309/java.13-4-4.
24. PITTIRUTI M., HAMILTON H., BIFFI R. et al. ESPEN guidelines on parenteral nutrition: central venous catheters (access, care, diagnosis and therapy of complications). Clin Nutr 2009; 28(4): 365–377. doi: 10.1016/j.clnu.2009.03.015.
25. PITTIRUTI M., LA GRECA A., SCOPPETTUOLO G. The electrocardiographic method for positioning the tip of central venous catheters. J Vasc Access 2011; 12(4): 280–291. doi: 10.5301/JVA.2011.8381.
26. PITTIRUTI M., BERTOLLO D., BRIGLIA E. et al. The intracavitary ECG method for positioning the tip of central venous catheters: results of an Italian multicenter study. J Vasc Access 2012; 13(3): 357–365. doi: 10.5301/JVA.2012.9020.
27. PITTIRUTI M., SCOPPETTUOLO G., DOLCETTI L. et al. Clinical use of Sherlock- 3CG® for positioning peripherally inserted central catheters. J Vasc Access 2019; 20(4): 356–361. doi: 10.1177/1129729818805957.
28. PITTIRUTI M., PELAGATTI F., PINELLI F. Intracavitary electrocardiography for tip location during central venous catheterization: a narrative review of 70 years of clinical studies. J Vasc Access 2021; 22(5): 778–785. doi: 10.1177/1129729820929835.
29. PITTIRUTI M., VAN BOXTEL T., SCOPPETTUOLO G. et al. European recommendations on the proper indication and use of peripheral venous access devices (the ERPIUP consensus): a WoCoVA project. J Vasc Access 2023; 24(1): 165–182. doi: 10.1177/11297298211023274.
30. REN X. L., LI H. L., LIU J. et al. Ultrasound to localize the peripherally inserted central catheter tip position in newborn infants. Am J Perinatol 2021; 38(2): 122–125. doi: 10.1055/s-0039-1694760.
31. SHEN Y., WANG G., SONG L. et al. A retrospective two-center cohort study on the use of routine chest X-ray after peripherally inserted central catheter placement under ultrasound and intracavitary electrocardiography guidance. Ann Transl Med 2022; 10(24): 1315. doi: 10.21037/atm-22-5417.
32. XIAO A. Q., SUN J., ZHU L. H. et al. Effectiveness of intracavitary electrocardiogram-guided peripherally inserted central catheter tip placement in premature infants: a multicentre pre-post intervention study. Eur J Pediatr 2020; 179(3): 439–446. doi: 10.1007/s00431-019-03524-3.
33. YIN Y. X., GAO W., LI X. Y. et al. Insertion of peripherally inserted central catheters with intracavitary electrocardiogram guidance: a randomized multicenter study in China. J Vasc Access 2019; 20(5): 524–529. doi: 10.1177/1129729818819732.
34. YU T., WU L., YUAN L. et al. The diagnostic value of intracavitary electrocardiogram for verifying tip position of peripherally inserted central catheters in cancer patients: a retrospective multicenter study. J Vasc Access 2019; 20(6): 636–645. doi: 10.1177/1129729819838136.
35. YUAN L., LI R., MENG A. et al. Superior success rate of intracavitary electrocardiogram guidance for peripherally inserted central catheter placement in patients with cancer: A randomized open-label controlled multicenter study. PLoS ONE 2017; 12(3): e0171630. doi: 10.1371/journal.pone.0171630.
36. ZHOU L., XU H., LIANG J. et al. Effectiveness of intracavitary electrocardiogram guidance in peripherally inserted central catheter tip placement in neonates. J Perinat Neonatal Nurs 2017; 31(4): 326–331. doi: 10.1097/JPN.0000000000000264.
Bc. Iveta Constantine, MSc.1
Magda Michaliková, DiS.2
PhDr. Andrea Polanská, MBA1
Zuzana Figurová2
Mgr. Adéla Kondé, Ph.D.3
1Útvar náměstka ředitele pro ošetřovatelskou péči, FN Ostrava
2PICC tým, FN Ostrava
3Katedra aplikované matematiky, Fakulta elektrotechniky a informatiky, VŠB – TU Ostrava
Recenze
MUDr. Vendelín Chovanec, Ph.D.
Angiointervenční oddělení, Radiologická klinika FN Hradec Králové
Další články v tomto čísle
- Editorial 5/2025
- Ústřední vojenská nemocnice nabízí všeobecným sestrám specializační vzdělávání v geriatrii
- „Průběh porodu nedefinuje vaši hodnotu jako ženy a matky,“ říká porodní asistentka Bc. Julie Bischofová
- Autonómia sestier, self-care a úskalia každodennej praxe
- Návrat domů po transplantaci plic: role sestry v podpoře domácí péče a psychosociální adaptace pacienta
- Žilní vstupy a jejich ošetřování
- Možnosti ošetrovateľstva v primárnej prevencií závislosti
- Opioidní terapie u popálených dětských pacientů: efektivita a bezpečnost
- Péče o pečující aneb Jak je důležitá podpora osob starajících se o pacienty na domácí umělé plicní ventilaci
- DOCTIS: Nový standard praktického lékařství














