


Číslo 4 / 2016
Evidence-based postupy v neurorehabilitaci spastické parézy
Neurorehabilitace hraje nezastupitelnou roli v organizaci péče o pacienty po získaném poškození mozku, k jejichž disabilitě nejvíce přispívají negativní příznaky syndromu horního motoneuronu. U těchto pacientů jsou rehabilitační postupy indikovány především ve vztahu k hlavním faktorům získané disability. Kombinace jednotlivých přístupů se mění v průběhu vývoje centrálních příznaků a zcela zásadní je odlišit terapeutický přístup v pseudochabém a ve spastickém stadiu.
Dokud se neobjeví svalová hyperaktivita, lze s dobrým efektem využívat široké spektrum komplexních terapeutických postupů. Jakmile u pacienta nastoupí spastické stadium, je nutné nejvíce postižené segmenty vyšetřovat a postupovat analyticky ve vztahu k funkci končetiny (kolektiv autorů, 2014). Komplexní léčbu pacientů s projevy syndromu centrálního motoneuronu (Gracies, 2005) – parézou, svalovou hyperaktivitou a zkrácením měkkých tkání – poskytujeme v Ústřední vojenské nemocnici – Vojenské fakultní nemocnici v Praze (ÚVN) v rámci Centra spasticity, kde realizujeme koncept léčby spastické parézy podle Jeana-Michela Graciese. Spektrem nemocných a cílovou skupinou jsou dospělí pacienti po získaném akutním poškození mozku. Především jsou to pacienti v různém stadiu po cévní mozkové příhodě s klinicky vyjádřenou spastickou parézou horní a dolní končetiny, dále po úrazech, tumorech atd.
Základem vyšetření je zhodnocení spastické parézy „Five-step clinical assessment in spastic paresis“ (Gracies, 2010). Vyšetřuje se v daných segmentech: 1. pasivní rozsah pohybu, 2. úhel zárazu nebo klonu a stupeň spasticity dle Tardieuho škály, 3. aktivní rozsah pohybu, 4. frekvence rychlých alternujících pohybů, 5. subjektivní a objektivní hodnocení funkce. Pro objektivní zhodnocení funkce paretické horní končetiny využíváme Modifikovaný Frenchayský test paže, který je založen na provedení deseti manuálních činností. Tento test je hodnocen na škále 0–10 (hodnotí se kvantita a kvalita provedeného úkolu). U dolní končetiny využíváme test rychlosti chůze na 10 m, který je modifikovatelný dle potřeb pacienta (chůze rychlá/pomalá, typ kompenzační pomůcky). Na základě provedených vyšetření vytipujeme klíčové svaly k cílené terapii. Racionální je soustředit se na konkrétní segment nebo funkci dle preferencí pacienta. Vzhledem k tíži postižení se zaměříme na horní nebo dolní končetinu. Po prvním sezení pacient odchází seznámen s postupem plánované terapie, systémem kontrol, svaly vytipovanými k případné aplikaci botulotoxinu a poučen o nutnosti denní autoterapie v podobě protahovacích cvičení (obr. 1) více spastických antagonistů a posilovacích cvičení více paretických agonistů. Zpravidla je léčba cílena na dva až tři svaly v preferovaných segmentech (Říha et al., 2015). Před nastavením léčebné strategie, v našem případě uceleného neurorehabilitačního programu, je nutné si ujasnit reálné cíle pacienta. Pro analýzu problémových oblastí využíváme na našem pracovišti Kanadské hodnocení výkonu zaměstnávání (z angl. Canadian Occupational Performance Measure, COPM), které je založeno na semistrukturovaném rozhovoru pacienta s terapeutem. Hodnocení se zaměřuje na tři základní oblasti: sebeobsluhu, produktivitu a volný čas. Na škále 1–10 hodnotí pacient subjektivně výkon, důležitost a spokojenost. Ve výsledku jde o identifikaci problémových oblastí a poté nastavení vhodných cílů terapie, ke které slouží Škála dosažení cíle (z angl. Goal attainment scailing, GAS). Jedná se o metodu stanovující subjektivní hodnoticí škálu s cílem kvantifikovat změnu funkčního stavu vzhledem k předem definovanému cíli (Kiresuk a Sherman, 1968, Říha a Dvořáková, 2015). Pacienti v rámci rehabilitačního procesu mají vyšší motivaci, pokud jsou jejich cíle zřetelně definovány a jsou ve shodě s požadavky na fungování v běžném životě (Hart a Evans, 2006, Sivaraman, 2003). Klademe důraz na aktivní spolupráci všech zúčastněných v rámci interprofesního týmu a pacienta, který je vázán dohodou o spolupráci a informovaným souhlasem (Gracies, 2010, Hoskovcová a Gál, 2012). Tato kombinace diagnostických a léčebných procedur, včetně intervenčních, tak vykazuje velmi dobrý efekt.
S odstupem jednoho měsíce provádíme kontrolní vyšetření v rámci rehabilitační konference za účasti indikujícího a aplikujícího lékaře, ergoterapeuta a fyzioterapeuta. Dle protokolu znovu testujeme trénované svaly, a pokud jsou k indikaci, následuje samotná aplikace botulotoxinu s využitím EMG stimulace (Říha a Dvořáková, 2015). Další kontroly probíhají na konci prvního a třetího měsíce od aplikace. V prvním měsíci lze pozorovat nejvyšší efekt aplikace, na konci třetího měsíce se očekává mírný pokles efektu, nikdy však neklesá na úplný výchozí funkční stav pacienta.
Terapie spastické parézy dle konceptu Jeana-Michela Graciese (Gracies, 2005 a 2010, Gál et al., 2015) by měla zahrnovat kombinaci následujících prvků:
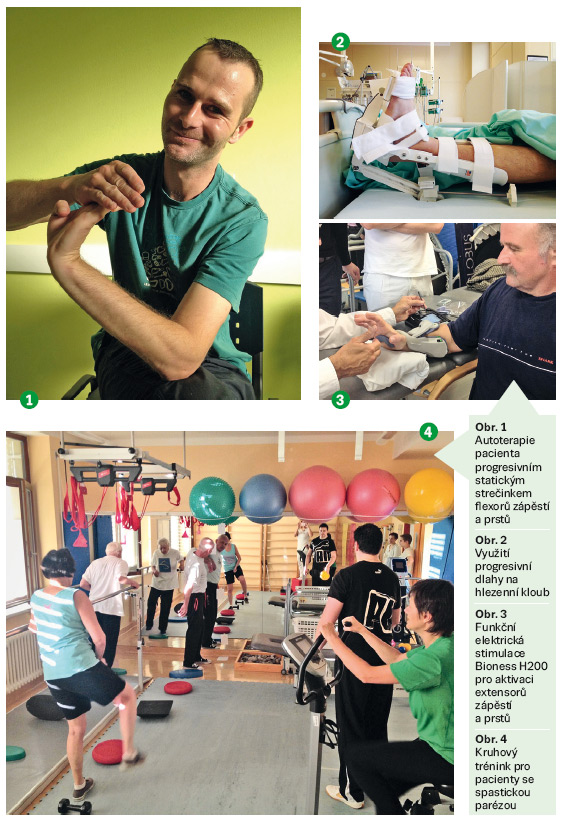
1. Progresivní prolongovaný statický strečink všech hyperaktivních a zkrácených svalů. Zkrácení svalů s rizikem rozvoje kontraktury je léčeno metodou statického progresivního prolongovaného strečinku, případně statickým progresivním dlahováním. Využití individuálně zhotovených progresivních dlah vidíme zejména v usnadnění ústavní péče (obr. 2). Jejich aplikace dvakrát denně na dobu 30 minut dle tolerance pacienta tak může probíhat i v rámci rehabilitačního ošetřování, které provádějí proškolené zdravotní sestry. Délka a intenzita strečinku pro jednotlivé svaly nebyla dosud jednoznačně stanovena, na základě empirie a některých studií lze však doporučit alespoň 10 minut, spíše však 30 minut na každou svalovou skupinu (Gál et al., 2015). Při provádění strečinku dbáme na autoterapii pacienta, pokud zásadně nelze, tak s využitím rodinného příslušníka.
2. Intenzivní motorický trénink vykonáváním vysokých počtů neasistovaných rapidních alterujících pohybů a funkčních cviků. Přehled rehabilitačních postupů, které mají v současné době dobrou evidenci k aktivaci neuroplastických změn uvádí kolektiv autorů (2014) následovně: intenzivní specifický trénink konkrétních činností, terapie zamezeného používání (CI-Terapie), zrcadlová terapie, cvičení v představě, kruhové tréninky, robotická rehabilitace, funkční elektrická stimulace a virtuální realita. Pro vhodná doporučení a použití jednotlivých rehabilitačních technik a postupů je důležitá průkaznost jejich efektivity podle požadavků medicíny založené na důkazech (evidence-based medicine). Některé postupy se sice běžně empiricky používají, jejich efektivita však ještě nebyla dostatečně prokázána.
K postupům, které nyní evidenci mají a vykazují výborný efekt v kombinaci s nitrosvalovou aplikací botulotoxinu typu A, patří např. funkční elektrická stimulace (Wilkenfeld, 2013). Jedná se o aplikace neuromuskulární stimulace souběžně s tréninkem zaměřeným na konkrétní úkol nebo výkon funkční aktivity. Elektricky indukované kontrakce extenzorů zápěstí a prstů ukázaly statistické i klinické zlepšení postižení paretické horní končetiny. V rámci funkčního tréninku lze s využitím funkční elektrické stimulace Bioness H200 trénovat úchopovou a manipulační funkci ruky, držení předmětu a jeho uvolnění v rámci výkonu běžných denních činností (Alon et al., 2008; obr. 3). Funkční elektrická stimulace je také moderní způsob terapie paretické dolní končetiny (Bioness L300 nebo L300 Plus), který slouží ke korekci pohybového deficitu. Využívá se zejména u pacientů s deficitem aktivní dorzální flexe v hlezenním kloubu a nestability kolenního kloubu. Ukázala se velmi efektivní na zvýšení rychlosti chůze, zlepšuje stabilitu chodidla při stojné fázi a má velmi dobrý tréninkový efekt (Johnson et al., 2004). Cvičení na přístrojích se zpětnou vazbou poskytuje pacientovi repetitivně trénink zábavnou formou, terapeutovi poskytuje objektivní zhodnocení výsledků terapie. V naší praxi využíváme např. Armeo Spring, což je robotický systém kompenzující gravitační tíhu horní končetiny a posilující motorické funkce paretické horní končetiny. Tyromotion Amadeo je systém pro cvičení prstů, který navíc umožňuje měření izometrické síly ruky a rozsahu pohybu prstů. Pro trénink dolní končetiny využíváme dynamický chodník Zebris, který slouží kromě nácviku chůze také k analýze a motivační zpětné vazbě. Pro pacienty se spastickou parézou dále organizujeme kruhové tréninky, které mají formu progresivní terapie. Zejména se jich účastní skupina 6–8 iktových pacientů a trénink je zaměřen na opakování a progresivní cvičení na úkol zaměřených aktivit (z angl. task-specific training; obr. 4). Doporučená intenzita kruhového tréninku je 90 minut 2× týdně po dobu 12 týdnů (van de Port, 2012). Hlavní důvody pro pořádání kruhových tréninků pro pacienty se spastickou parézou jsou následující: jedná se o cvičení smysluplnou a progresivní cestou k dosažení stanovených cílů, efektivní využití času pro pacienty, podpora skupinové dynamiky (podpora, sociální interakce; Wevers, 2009). Trénink funkčních cviků vede ke zlepšení mobility, stereotypu chůze, zlepšení rovnováhy, nácvik pohybu v reálném prostředí, zlepšení funkce hemiparetické končetiny, zvýšení aerobní kapacity pacientů a celkové kondice. Frimpong et al. (2014) dokonce uvádí, že kruhový trénink pro iktové pacienty může bezpečně nahradit klasickou ambulantní formu fyzioterapie pacientů, kteří jsou propuštěni z ústavní léčby a vyžadují další funkční trénink. Také terapie virtuální realitou má svoji evidenci ke zlepšení paretických končetin. Využití Xbox a Kinectu pomáhá pacientovi zlepšit nejen motorické funkce, ale také poskytuje terapii zábavným způsobem. Pacienti se mohou vcítit do různých aktivit v rámci trojdimenzionální reality a tato terapie vede k rychlejšímu uzdravení subakutních pacientů po iktu (Bao et al., 2013). Existence studií prokazuje signifikantní zlepšení motorických deficitů v rámci srovnání Fugl-Meyerova skóre před a po terapii využívající Xbox (Housman et al., 2009, Piron et al., 2010) a také v rámci zlepšení rovnováhy pacienta (Lange, 2011). Využití virtuální reality se ukazuje také jako vhodná domácí autoterapie.
Na závěr můžeme optimisticky konstatovat, že je především na nás, jakým způsobem uvádíme do praxe moderní trendy v duchu medicíny založené na důkazech podložené zkušenostmi. Ze zkušenosti vyplývá, že pro výsledný léčebný efekt v rehabilitaci je rozhodující řádná diagnostika a klasifikace dle standardizovaného vyšetřovacího protokolu. Následně cílená aplikace léčiva za podpory pohybové terapie. Je otázkou času, kdy spíše než tradiční, empirické přístupy a úcta k nim bude naše rehabilitace postavena na seriózních, důkazy podložených konceptech a metodách.
Mgr. Tereza Sádlová, MUDr. Petra Dvořáková, Oddělení rehabilitace a fyzikální medicíny, ÚVN Praha, MUDr. Michal Říha, PhD., MBA, Oddělení rehabilitace a fyzikální medicíny, Neurochirurgická a neuroonkologická klinika 1. LF UK a ÚVN Praha
Literatura:
1. Kolektiv autorů. Metodická příručka pro odborníky pracující v oblasti neurorehabilitace [online]. Praha: Erudis o. p. s., 2014, s. 1–28
2. Gracies JM. Pathophysiology of spastic paresis I: Paresis and soft tissue changes. Muscle Nerve. 2005;31(5):535–551
3. Gracies JM et al. Five-step clinical assessment in spastic paresis. Eur. J. Phys. Rehabil. Med. 2010;46(3):411–421
4. Říha M, Dvořáková P, Sádlová T. Moderní trendy v léčbě fokální spastické parézy po získaném poškození mozku. Practicus. 2015;14(09):19–22
5. Hoskovcová M, Gál O. Rehabilitace a spasticita. In Štětkářová I, Ehler E, Jech R (eds.). Spasticita a její léčba. Praha: Maxdorf, 2012, s. 177–212
6. Kiresuk TJ, Sherman RE. Goal attainment scaling: A general method for evaluating comprehensive community mental health programs. Community Mental Health Journal. 1968;4(6):443–453. [online]. [cit. 2016-01-02]. DOI: 10.1007/bf01530764
7. Hart T, Evans J. Self-regulation and Goal Theories in Brain Injury Rehabilitation. Journal of Head Trauma Rehabilitation 2006;21(2):142–155. [online]. [cit. 2016-02-03]. DOI: 10.1097/00001199-200603000-00007
8. Sivaraman NKP. Life goals: the concept and its relevance to rehabilitation. Clinical Rehabilitation 2003;17(2):192–202. [online]. [cit. 2016-02-03]. DOI: 10.1191/0269215503cr599oa
9. Říha M, Dvořáková P. Goal Attainment Scaling (GAS) – metoda hodnocení efektu terapie u pacientů s fokální spastickou parézou. Rehabilitace a fyzikální lékařství. 2015;22(3):144–147
10. Říha M, Dvořáková P. Léčba fokální spastické parézy po získaném poškození mozku – zkušenosti z rehabilitačního pracoviště. Rehabilitace a fyzikální lékařství. 2015;22(3):140–143
11. Gál O, Hoskovcová M, Jech R. Neuroplasticita, restituce motorických funkcí a možnosti rehabilitace spastické parézy. Rehabilitace a fyzikální lékařství. 2015;22(3):101–127
12. Wilkenfeld AJL. Review of electrical stimulation, botulinum toxin, and their combination for spastic drop foot. J. Rehabil. Res. Dev. 2013;50(3):315–326
13. Alon G, Levitt AF, McCarthy P. Functional Electrical Stimulation (FES) may modify the poor prognosis of stroke survivors with severe motor loss of the upper extremity. Am. J. Phys. Med. Rehabil. 2008;87(8):627–636
14. Johnson C, Burridge JH, Strike PW. The Effect of Combined Use of Botulinum Toxin Type A and Functional Electric Stimulation in the Treatment of Spastic Drop Foot After Stroke: A Preliminary Investigation. Arch. Phys. Med. Rehabil. 2004;85:902–909
15. Van De Port I, Wevers L, Lindeman E et al. Effects of circuit training as alternative to usual physiotherapy after stroke: randomised controlled trial. BMJ. 2012;344:e2672
16. Wevers L, Van De Port I, Vermue M. Effects of task-oriented circuit class training on walking competency after stroke. Stroke. 2009;40:2450–2459. DOI: 10.1161/STROKEAHA.108.541946
17. Frimpong E, Olawale OA, Antwi DA. Task-oriented circuit training improves ambulatory functions in acute stroke: a randomized controlled trial. Journal of Medicine Sciences. 2014;5(8):169–175
18. Bao X, Mao YR, Lin Q, Qiu YH, Chen SZ, Li L, Cates RS, Zhou SF, Huang DF. Mechanism of Kinect-based virtual reality training for motor functional recovery of upper limbs after subacute stroke. Neural Regen Res. 2013;8(31):2904–2913
19. Housman SJ, Scott KM, Reinkensmeyer DJ. A randomized controlled trial of gravity-supported, computer-enhanced arm exercise for individuals with severe hemiparesis. Neurorehabil Neural Repair. 2009;23(5):505–514
20. Piron L, Turolla A, Agostini M et al. Motor learning principles for rehabilitation: a pilot randomized controlled study in poststroke patients. Neurorehabil Neural Repair. 2010;24(6):501–508
21. Lange B, Chang CY, Suma E et al. Development and evaluation of low cost game-based balance rehabilitation tool using the microsoft Kinect sensor. Conf. Proc. IEEE Eng. Med. Biol Soc. 2011;2011:1831–1834
Další články v tomto čísle
- Zdržujte se hříšné nečinnosti, aby vás nestáhla tíží svou do hlubokosti pekelné (Karel IV.).
- Pomáhající profese si zaslouží úctu společnosti
- Sestry – manažerky a jejich role při řízení rizik (část 3)
- Základy arteterapie – Rozšířené vydání
- Rodičům na nejhezčí cestu
- Štandardizácia v ošetrovateľstve
- První pomoc pro každého – 2. doplněné vydání
- Rehabilitační centrum v berounské nemocnici oceňují odborníci i laici
- Fyzioterapie v praxi
- Balneologie v Lázních Bechyně











