


Číslo 9 / 2013
Afterdrop effect u pacientů v mírné hypotermii při mimotělním oběhu
Souhrn: V průběhu mimotělního oběhu řízeně upravujeme tělesnou teplotu nemocného z normotermie do mírné hypotermie a zpět. Manipulace s teplotou vyžaduje přesné a spolehlivé monitorování a účinné prostředky k ochlazování a následnému ohřevu organismu. Nežádoucím stavem při ohřívání je afterdrop effect, pokles teploty těla ovlivněný postupným uvolněním periferního krevního řečiště a vyrovnáváním teplot proudící krve organismem. Zajímá nás nejoptimálnější postup ohřívání v poslední fázi mimotělního oběhu, kterou je intenzivní vaskulární ohřívání.
Klíčová slova: mimotělní oběh – afterdrop effect – hypotermie.
Afterdrop effect in patients with mild hypothermia during extracorporeal circulation
Summary: During the extracorporeal circulation procedure we regulate body temperature of the patient from normothermia to mild hypothermia and back. Handling temperature requires accurate and reliable monitoring and efficient means of cooling and subsequent heating of the body. Undesirable state when heating is afterdrop effect decrease in body temperature affected by removing the peripheral bloodstream and balancing the temperature of blood flowing through the body. We are interested in optimal heating process in the last stage of extracorporeal circulation which is an intense vascular warming.
Keywords: extracorporeal circulation – afterdrop effect – hypothermia.
Úvod
1. Tělesná teplota
Tělesná teplota je velmi důležitou složkou perioperační a pooperační péče u srdečních operací. Rozlišujeme tělesnou teplotu centrální (teplota jádra) a teplotu periferie (pláště). Protože se během hypotermického mimotělního oběhu (MO) mění teplota organismu nerovnoměrně, je nutné sledovat teplotu tělesného jádra i teplotu periferie.
1.1 Teplota tělního jádra
Teplota vitálních orgánů – srdce, mozku, jater a ledvin. Tyto orgány se vyznačují intenzivním metabolismem, tedy i větší produkcí tepla. Během ochlazování krve v oxygenátoru klesá teplota tělesného jádra mnohem rychleji než teplota periferie. Dochází k opačnému stavu, než je fyziologický – centrální teplota je nižší než periferní. Náhlé ochlazení jádra způsobí intenzivní periferní vazokonstrikci, čímž je snížen průtok krve periferií.
1.2 Teplota periferie
Periferní teplota se pohybuje ve velkém rozmezí v závislosti na termoregulačním mechanismu. Vzhledem k tomu, že periferie (kůže, tuková tkáň, svaly, kosti) funguje jako jakýsi rezervoár tepla, je zde v důsledku vazokonstrikce snížen průtok krve, což má za následek podstatně pomalejší ochlazení periferních částí. Zároveň zde začíná probíhat anaerobní metabolismus jako důsledek snížení přísunu kyslíku do tkání. Důsledkem je pak rozvoj metabolické acidózy. Svalová hmota je mezičlánkem mezi teplotou jádra a teplotou periferie. Chladí se pomaleji než jádro, ale rychleji než periferie.
2. Hypotermie
Hypotermie je pokles teploty tělesného jádra pod teplotu 35 °C. Hloubka hypotermie je definována podle následujícího rozdělení:
- Mírná (mild) hypotermie 35–32 °C,
- Střední (moderate) hypotermie 31–26 °C,
- Hluboká (deep) hypotermie 25–20 °C,
- Velice hluboká (profound) 19–14 °C.
2.1 Důvody zavedení hypotermie při srdečních operacích
Důvody pro navození hypotermie jsou:
- zpomalení tkáňového metabolismu,
- zachování energetických zásob,
- snížení orgánové spotřeby kyslíku.
Cílem všech zmíněných důvodů je zvýšit toleranci orgánů k hypoxii při jejich případné ne zcela adekvátní perfuzi během MO. Bylo prokázáno, že s každým poklesem teploty organismu o 10 °C klesá spotřeba kyslíku přibližně o 50 %. Vyjádříme-li tuto závislost číselně, klesá spotřeba kyslíku ze 120 ml/m² při TT 37 °C na 33 ml/m² při TT 20 °C. Snížení průtoku orgány ale není rovnoměrné. K největší redukci průtoku dochází v příčně pruhované svalovině a končetinách, dále následují ledviny, oblast splanchniku, srdce a mozek. Při tomto snížení průtoku je zásobení příslušných tkání kyslíkem přiměřené metabolické aktivitě příslušného orgánu.
3. Možnosti monitorování tělesné teploty
Distální jícen
Teplota v dolním jícnu nejvíce odpovídá teplotě krve v aortě (teplotě jádra). Tato teplota však může být v průběhu MO zkreslená aplikací chlazené krevní kardioplegie a podáním ledové tříště do perikardiálního vaku.
Nasopharynx
Teplota v této oblasti reprezentuje teplotu vdechovaných plynů. Tato teplota odráží mozkovou teplotu během MO. Při rychlém ohřívání může snadno vzniknout mezi termistorem a mozkem gradient 1 až 3,4 °C. Podhodnocení teploty může vést k hypertermii mozku, zhoršení kyslíkové balance a prohloubení mozkové ischémie.
Močový měchýř
Měření v močovém měchýři poskytuje velmi kvalitní informace o teplotě jádra. K měření se používá močová cévka s integrovaným teplotním čidlem.
Kůže
Teplota kůže záleží na prokrvení podkoží. Je ovlivněna pocením a sáláním. Teplotu monitorujeme nejlépe kontinuálně elektronickými přístroji, které měří i nízké hodnoty.
Rektum
Používáme pro měření teploty periferie. Při zavedení teploměru příliš hluboko může dojít ke zkreslené hodnotě u nedostatečně vyprázdněného pacienta. Pokud je teploměr zaveden mělce, může během operace opustit konečník.
Vnější zvukovod
Teplota ve vnějším zvukovodu odpovídá relativně přesně teplotě krve proudící do mozku. Při zavádění sondy je však nebezpečí perforace bubínku. Měření může být zkresleno přítomností ušního mazu, který působí jako izolátor.
Plicnice
V arterii pulmonalis monitorujeme centrální teplotu. Tato teplota se měří pomocí termistoru v plicnicovém katetru. Během MO je při srdeční zástavě omezen průtok krve plicnicí, proto není v této fázi výsledek měření vhodný k hodnocení centrální teploty.
Teplota krve v tepenné lince MO
Teplota mozkové tkáně téměř dokonale kopíruje teplotu krve v tepenné lince, pokud je arteriální linka zavedená v ascendentní aortě. Tuto teplotu měříme na oxygenátoru, kde jsou výstupy pro teploměrné sondy.
Teplota krve v žilní lince MO
Tato teplota odráží teplotu tělesného jádra. Sledujeme ji ke stanovení teplotního rozdílu mezi vodou, krví a pacientem při ohřívání. Teplotní gradient nesmí přesáhnout 10 °C! Vyšší gradienty nesou riziko vzniku mikroembolizace způsobené odlišnou rozpustností plynů v krvi při různých teplotách.
4. Ohřívání nemocného
4.1 Možnosti ohřívání nemocného na operačním sále
Ve výměníku tepla oxygenátoru dosáhne teplota krve normální hodnoty za poměrně krátkou dobu. To znamená, že i teplota tělesného jádra se rychle vrací k normálu. Ohřívání periferie se však, podobně jako při ochlazování pacienta, za ohříváním tělesného jádra zpožďuje.
V periferii (cévy ve svalech, podkoží a kůži) přetrvává vazokonstrikce. Na konci mimotělního oběhu mohou být tyto tkáně ještě nedostatečně prohřáté. Toto zpoždění může být i v závislosti na tělesné konstituci pacienta výrazné a pro nemocného v následné pooperační péči i nebezpečné. Pokud ukončíme mimotělní oběh s centrální teplotou 37 °C a periferie nebude dostatečně prohřátá, poklesne hodnota centrální teploty o 2–3 °C, než se stabilizuje.
Výměník tepla je součástí každého oxygenátoru. Je umístěn vždy před oxygenátorem, aby nedošlo k uvolňování mikrobublin plynů z okysličené krve při ohřívání. Výměník je konstruován tak, že na jedné straně proudí voda a na druhé straně proudí krev. Obě tekutiny jsou neprodyšně odděleny tepelně vodivým materiálem. Zdrojem teplé a studené vody je tepelná jednotka.
Při ohřívání nemocného využíváme ohřívací podložku, která je umístěna pod pacientem po celé délce operačního stolu. Tato podložka je propojena s tepelnou jednotkou výměníku tepla.
Současně přihříváme přenosným ohřívadlem s flexibilní hadicí, kterou můžeme přivádět teplý vzduch k tělu pod operačním rouškováním, na operačním sále se zvýší teplota. Pokud je teplota na operačních sálech nižší než 21 °C, pacienti v celkové anestezii prochládají.
K prochládání přispívají i následující faktory:
- otevřené velké tělesné dutiny – ztráty vypařováním,
- přívod velkého objemu chladných infuzí a krevních přípravků,
- vyšší věkové skupiny mají nižší prahové hodnoty pro vazokonstrikci.
4.1.1 Ohřívací jednotky infuzních a transfuzních derivátů
Tyto jednotky ohřívají roztoky nebo deriváty před vstupem do organismu, a to ponořením do vodní lázně nebo ohříváním protékajícího roztoku k tomu určeným infuzním setem, který je omýván proudící teplou vodou. Na obou přístrojích lze nastavit požadovanou teplotu. Po jejím dosažení zazní akustický signál upozornění.
4.2 Možnosti ohřívání nemocného na jednotce pooperační a resuscitační péče (dále JPRP)
Na JPRP má každý pacient po příjezdu ze sálu napojeno přenosné ohřívadlo do přikrývky, dokud se jeho tělesná teplota nestabilizuje.
5. Metodika
Kritéria pro výběr měřených pacientů
Pro naše měření vývoje teplot v časovém odstupu jsme měly k dispozici 10 ks močových cévek s termistorem. Zkoumanou skupinu jsme rozdělily na 5 mužů a 5 žen. Věkový rozptyl jsme určily 55–65 let. Jednalo se o skupinu, v níž jsme předpokládaly, že nebude v závažné míře zastoupeno poškození cévního řečiště ztrátou elasticity kornatěním a zúžením cév. Tato onemocnění patří mezi faktory, které ovlivňují aktivní posun teplot tělesného jádra a hlavně periferie. Plocha povrchu těla BSA (body surface area) se u vybraných pacientů pohybovala v rozmezí 1,65–2,24 m2. Do výběru byli zařazeni muži s tělesnou výškou 170–190 cm a tělesnou hmotností 80–100 kg a ženy s tělesnou výškou 150–170 cm a hmotností 60–80 kg.
5.1 Postup při ohřívání
Nemocné jsme rozdělili do dvou skupin:
- skupina ohřívaná maximální počáteční teplotou 38,5 °C a s dobou ohřevu nad 45 min.;
- skupina ohřívaná maximální počáteční teplotou 40 °C a s dobou ohřevu do 45 min.
5.2 Skupina ohřívaná max. počáteční teplotou 38,5 °C
Tato skupina pacientů byla ohřívána pomalejším způsobem. Při začátku ohřevu byla na tepelné jednotce nastavena teplota 38,5 °C. Tato teplota byla udržována, dokud teplota v arteriálním systému nedosáhla 38 °C. Po dosažení této teploty byla teplota na tepelné jednotce korigována tak, aby teplota v arteriálním systému nepřesáhla teplotu 38 °C. Pacient byl od začátku současně ohříván jak výměníkem tepla, tak pomocí ohřívací podložky a přenosného ohřívadla. Ohřívací podložka byla vyhřívána stejnou teplotou jako výměník tepla. Na přenosném ohřívadle byla nastavena teplota 38–40 °C.
5.3 Skupina ohřívaná max. počáteční teplotou 40 °C
Tato skupina pacientů byla ohřívána rychlejším způsobem. Při začátku ohřevu byla na tepelné jednotce nastavena teplota 40 °C. Tato teplota byla udržována, dokud teplota v arteriálním systému nedosáhla 38 °C. Po dosažení této teploty byla teplota na tepelné jednotce korigována tak, aby teplota v arteriálním systému nepřesáhla teplotu 38 °C. Další pomůcky k ohřevu byly totožné jako u skupiny 38,5 °C.
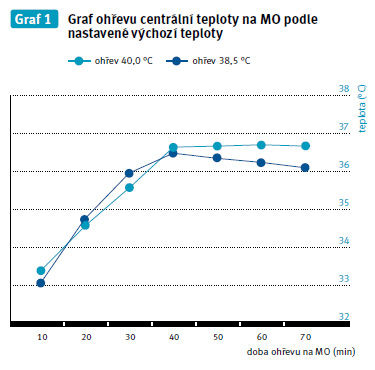
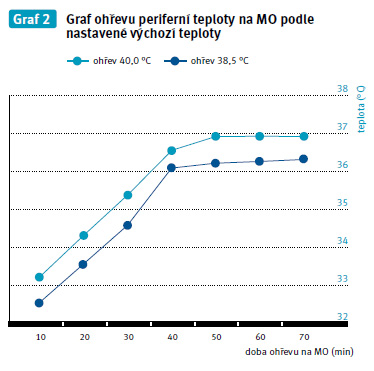
6. Grafy naměřených hodnot
Viz graf 1, 2.
7. Vyhodnocení
7.1. Vyhodnocení měření s maximální teplotou ohřevu 38,5 °C
Pacienti ohřívaní hodnotou 38,5 °C dosáhli průměrné centrální teploty při ohřevu během mimotělního oběhu v době odjezdu ze sálu 36,1 °C. U pacientů jsme sledovaly celkový stav, diuréza byla udržována průměrně 150 ml/hod., takže hodnoty měřené v močovém měchýři můžeme hodnotit jako významově správné. K nižší tělesné teplotě se vážou komplikace s krvácením. U tří pacientů z pěti sledovaných se objevily pooperační ztráty v rozmezí 150–200 ml a hodnota aktivovaného koagulačního testu ACT (Activated Clotting Time) byla u všech sledovaných zvýšená 130–180 sekund. Hodnoty naměřené na JPRP nám dokazují, že pacienti udrželi svoji tělesnou teplotu během převozu ze sálu a nárůst teploty jen s přenosným ohřívadlem byl velmi pozvolný. Měřením jsme vyhodnotily ohřev teplotou 38,5 °C jako nevýhodný.
7.2 Vyhodnocení měření s minimální teplotou ohřevu 40 °C
Pacienti ohřívaní touto teplotou dosáhli průměrné centrální teploty při ohřevu během mimotělního oběhu v době odjezdu ze sálu 36,7 °C. Tato teplota byla optimální pro další vývoj pooperačního stavu. Nedocházelo k nadměrnému krvácení z operačního pole, hodnoty ACT byly v rozmezí 99–110 sekund a obsah drénů z operační rány byl v době odjezdu ze sálu 0–50 ml. Na oddělení JPRP nedošlo k větším krevním ztrátám. V pooperačním období jsme nezaznamenaly výskyt komplikací v oblasti hojení operační rány. Dle grafu není patrné, že by u pacientů docházelo k afterdrop effectu. Začátek ohřívání s nastavením teploty 40 °C na ohřívací jednotce jsme vyhodnotily jako pro pacienta optimální.
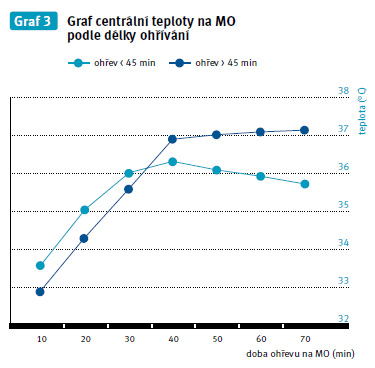
7.3 Vyhodnocení měření podle časů ohřívaní do 45 minut
Z naměřených výsledků můžeme potvrdit, že pacienti ohřívaní do 45 minut v době MO opouštěli operační sál s průměrnou centrální teplotou 35,7 °C. Tato teplota může být zdrojem již výše zmíněných komplikací souvisejících s dosaženou nižší tělesnou teplotou.
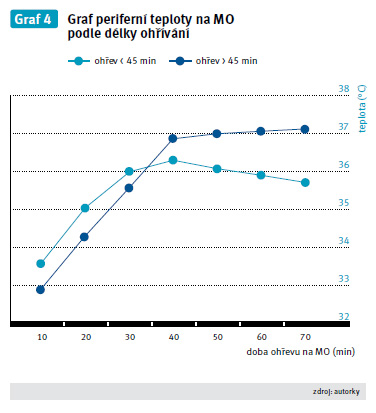
7.4 Vyhodnocení měření podle času ohřívání nad 45 minut
Pacienti, kteří byli ohříváni po dobu delší než 45 minut, opouštěli operační sál s průměrnou centrální hodnotou 37,1 °C. Teplota periferie na konci měření, tzn. po 120 minutách pobytu pacienta na oddělení pooperační péče, byla u odlišně ohřívaných pacientů rozdílná o 0,7 °C. Dosaženou teplotu je organismus schopen udržet a dále ji zvyšovat, ale než dosáhne optimální teploty, může dojít ke krvácivým komplikacím, které prodlužují pobyt na sále a zvyšují pravděpodobnost pooperačních komplikací v oblasti hojení ran.
8. Diskuze
Na perioperačním a pooperačním průběhu ohřívání spolupracuje celý tým, každý jednotlivec může svou prací ovlivnit způsob nebo čas k zajištění komfortních podmínek pro pacienta. Spojení praktických zkušeností a měření nám poskytlo informace pro zvolení optimálního postupu ohřevu z mírné hypotermie.
Operatér informuje tým, že může začít s aktivním ohříváním pacienta, perfuziolog sleduje vývoj operace a zajímá se o včasné spuštění ohřevu. Výměník tepla je nastaven na 40 °C a ohřívá proudící krev v oxygenátoru a podušku pod pacientem. Teplota ohřívané krve by neměla přesáhnout 38 °C. Pod operační rouškování zavedeme hadici přenosného ohřívače. Teplota vzduchu z ohřívače se pohybuje v rozmezí 37–40 °C. V případě, že ohřev nepostupuje dle našich předpokladů, rizikovými faktory jsou obezita, ateroskleróza a ischemická onemocnění, je na zvážení podání léků s vazodilatačním účinkem. Chirurg bezpečně a bez průtahů zavře operační ránu. Rychlý transport pacienta na JPRP, kde se pokračuje v ohřívání, snižuje riziko prochladnutí.
Závěr
Cílem tohoto projektu bylo získat informace k ohřevu pacientů z hypotermie. Po vyhodnocení teplotních křivek získaných během mimotělního oběhu, pobytu na sále a oddělení pooperační péče jsme došly k závěru, že pro nemocné je nejvýhodnější, aby v závěru mimotělního oběhu dosáhli co nejvyšší tělesné teploty. Dosaženou teplotu je organismus schopen udržet bez výraznějšího poklesu časným převozem z operačního sálu na JPRP. Naměřené hodnoty dokazují, že k afterdrop efektu u operovaných v mírné hypotermii dochází, a po měření dokážeme odpovědět, jak by měl vypadat ideální postup ohřívání pacientů. S těmito výsledky jsme seznámily operační týmy, aby byly vytvářeny nejoptimálnější podmínky v perioperační a pooperační péči o nemocné.
Na závěr bychom chtěly poděkovat sestrám JPRP KCHO za jejich obětavou spolupráci.
Bc. Marcela Škabradová, jednotka klinické perfuze, Kardiocentrum, Nemocnice Na Homolce, Praha
Bc. Vladislava Jarošová, jednotka klinické perfuze, Kardiocentrum Nemocnice Na Homolce, Praha
Literatura:
1. Lonský V. Mimotělní oběh v klinické praxi. Praha: Grada Publishing, 2004, 215 s. ISBN 8024706539.
2. Larsen R et al. Anestezie. Praha: Grada Publishing, 1998, 739 s.
3. Wagner R. Kardioanestezie a perioperační péče v kardiochirurgii. Praha: Grada Publishing, 2009, 336 s. ISBN 978-80-247-1920-7.
4. Kaplan JA et al. Cardiac Anesthesia, 5th edn. Philadelphia: Elsevier Saunders, 2006.
Recenzovali:
MUDr. Oldřich Růžička – ZZS SČK, lékař
Mgr. Martina Červenková – vedoucí laboratoře Cord Blood Center CZ, s. r. o.
Bc. Michaela Novotná – Urologická klinika, VFN v Praze
Další články v tomto čísle
- Úsměv je svátek obličeje
- Mám příliš mnoho nabídek
- Kdyby na Měsíci byla jediná kapka rosy, která vám pomůže, přinesete ji
- Jak efektivně předcházet nemocničním infekcím
- MRSA (bariérový ošetřovatelský režim)
- Operace mozku při plném vědomí pacienta dělají i na Homolce
- Kazuistika dítěte s adnátní sepsí po porodu
- Práce klinického perfuziologa a kritické situace během mimotělního oběhu
- Návrh na zlepšení interní komunikace ve zdravotnickém zařízení
- Těhotenství a preventivní gynekologická péče u žen imigrantek











